FDA chấp thuận thuốc điều trị chứng chảy nước bọt mạn tính ở trẻ em
Ngày đăng: 03/08/2010

Lượt xem: 8233
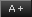
Cơ quan quản lý Thực phẩm và Dược Hoa Kỳ đã phê duyệt Cuvposa (glycopyrrolate) (dung dịch uống) để điều trị chảy nước bọt nghiêm trọng mạn tính do rối loạn thần kinh ở trẻ em độ tuổi từ 3 đến 16 tuổi.
Chảy nước bọt ở trẻ sơ sinh là bình thường. Nhưng tỷ lệ đáng kể trong số người tàn tật đều từng bị chảy nước bọt nguyên nhân chính do rối loạn chức năng thần kinh cơ và gây ra tình trạng khó nuốt. Cuvposa làm giảm chảy nước bọt bằng cách giảm sản xuất lượng nước bọt.

Glycopyrrolate đã được chấp thuận nhiều thập kỷ trước đây để điều trị viêm loét dạ dày và giảm tiết nước bọt ở những bệnh nhân bị gây mê. Cho đến nay, glycopyrrolate đã được sử dụng trong chỉ định chưa được FDA công nhận (off-label) để điều trị chảy nước bọt cho những người tàn tật, nhưng trong một hình thức liều lượng khác với các sản phẩm được phê duyệt. Một loại thuốc được cho là được sử dụng off-label khi bác sĩ sử dụng thuốc theo một cách khác hơn so với mô tả trong các nhãn thuốc chuẩn FDA phê duyệt.
Năm 2001, FDA đã tổ chức một cuộc họp ủy ban cố vấn để thảo luận về cách tốt nhất để phát triển sản phẩm thử nghiệm trong điều trị chảy nước bọt ở trẻ em có rối loạn thần kinh phù hợp với đạo đức và khoa học. Qua những thông tin tư vấn, FDA có thể hướng tới việc giải quyết các nhu cầu của những đối tượng này.
John Jenkins, MD, giám đốc của Văn phòng Dược phẩm mới ở Trung tâm đánh giá và nghiên cứu thuốc của FDA nói "Cuvposa cung cấp một liệu pháp quan trọng để kiểm soát tiết nước bọt ở những bệnh nhân bị bệnh thần kinh". "FDA chấp thuận không chỉ đảm bảo rằng sản phẩm đáp ứng tiêu chuẩn hiện đại về an toàn, hiệu quả, chất lượng và toa thuốc và nhãn, nhưng, cũng có kết quả khi dùng liều phù hợp hơn cho đối tượng bệnh nhân này."
Các thuốc FDA chấp thuận luôn được xem xét lại thông tin sản phẩm cụ thể. Điều này rất quan trọng để bảo đảm an toàn và hiệu quả của một thuốc thành phẩm. Ví dụ, người nộp đơn phải chứng minh rằng quy trình sản xuất đáng tin cậy, có thể sản xuất sản phẩm thuốc như chất lượng đã đăng ký, điểm mạnh, chất lượng và độ tinh khiết. FDA xem xét các nhãn thuốc của người nộp đơn đảm bảo rằng các chuyên gia y tế và bệnh nhân có các thông tin cần thiết để hiểu những rủi ro của một sản phẩm thuốc, độ an toàn và hiệu quả sử dụng.
Khi sử dụng chỉ định ngoài thông tin được FDA chấp thuận (off label), viên nén uống glycopyrrolate phải được nghiền nát để điều trị chảy nước bọt ở trẻ em bị rối loạn thần kinh. Cuvposa là một dung dịch uống có hương vị giúp trẻ dễ dàng hơn trong sử dụng và cung cấp liều lượng tối ưu cho từng bệnh nhân.
Trong các thử nghiệm lâm sàng của dung dịch uống Cuvposa glycopyrrolate, 78 phần trăm trẻ em dùng thuốc đạt cải thiện lâm sàng trong chứng chảy nước bọt so với 19 phần trăm sử dụng dụng giả dược.
Phản ứng bất lợi thường gặp của glycopyrrolate được báo cáo là khô miệng, táo bón, đỏ bừng, và bí tiểu (urinary retention) .
Dung dịch uống Cuvposa (glycopyrrolate) được phân phối ra thị trường bởi công ty dược phẩm Shionogi Pharma Inc của
Đăng bởi: Ds.Hoàng Thùy Linh
Các tin khác

THÔNG TIN THUỐC THÁNG 5 / 2013 21/08/2013

THÔNG TIN THUỐC THÁNG 6 / 2013 21/08/2013












(1).png)

.jpg)

.jpg)


.jpg)

.png)
.png)

.png)
.png)


